子宫内膜癌是由什么原因引起的?
子宫内膜癌的病因不十分清楚。多数作者认为内膜癌有两种类型,可能有两种发病机制。一类较年轻些,在无孕酮拮抗的雌激素长期作用下,子宫内膜发生增生性改变,最后导致癌变,但肿瘤分化较好;另一类发病机制不清楚,可能与基因变异有关,多见于绝经后老年人,体型瘦,雌激素水平不高。在癌灶周围可以是萎缩的子宫内膜,肿瘤恶性度高,分化差,预后不良。
前一类占子宫内膜癌的大多数,长期的无孕酮拮抗的雌激素刺激可能是主要发病因素。许多年前,人们就知道,给实验动物雌激素,观察到子宫内膜细胞有丝分裂增多,可引起子宫内膜由增生过长到内膜癌的演变,而给予孕激素则可减少内膜细胞的有丝分裂。长期持续的雌激素刺激 子宫内膜在雌激素的长期持续刺激、又无孕激素拮抗,可发生子宫内膜增生症,也可癌变。体制因素 内膜癌易发生在肥胖,高血压,糖尿病,不孕或不育及绝经的妇女。遗传因素 约20%内膜癌患者有家族史。目前,对子宫内膜癌的病因仍不十分清楚,根据临床资料与流行病学研究结果,子宫内膜癌的发生机制可分为两类:雌激素依赖型和非雌激素依赖型。
子宫内膜癌多见于以下高危因素:
1.无排卵 如伴有无排卵型或黄体功能不良的功能性子宫出血者,长期月经紊乱,使子宫内膜持续受雌激素刺激,无孕酮对抗或孕酮不足,子宫内膜缺少周期性改变,而长期处于增生状态。
2.不育 不育,尤其是卵巢不排卵引起的不育,患内膜癌的危险性明显升高。在子宫内膜癌患者中,约15%~20%的患者有不育史。这些患者因不排卵或少排卵,导致孕酮缺乏或不足,使子宫内膜受到雌激素持续性刺激。妊娠期间胎盘产生雌、孕激素,使子宫内膜发生相应的妊娠期改变;哺乳期,由于下丘脑和垂体的作用,使卵巢功能暂时处于抑制状态,使子宫内膜免于受雌激素刺激。而不孕者,尤其是因无排卵引起的不孕,使子宫内膜长期处于增生状态。
3.肥胖 肥胖,尤其是绝经后的肥胖,明显地增加了子宫内膜癌的危险性。绝经后卵巢功能衰退,而肾上腺分泌的雄烯二酮可在脂肪组织内经芳香化酶作用转化为雌酮,脂肪组织越多,转化能力越强,血浆中雌酮水平也越高。雌酮是绝经后妇女身体中主要的雌激素,子宫内膜是雌激素的靶器官,子宫内膜长期受到无孕激素拮抗的雌酮的影响,可导致内膜由增生到癌变。某些基础研究也指出,如增加了雄烯二酮到雌酮的转换,也就增加了内膜由增生到癌变的发生率。有人统计,按标准体重,超重9~23kg,患内膜癌的危险性增加了3倍,如超重>23kg,则危险性增加10倍。
一般将肥胖-高血压-糖尿病,称为子宫内膜癌三联征。北京医科大学第一附属医院妇产科于1970~1991年共收治以手术为主要治疗的子宫内膜癌患者153例,其中20%伴肥胖,44.4%患高血压,11.1%患糖尿病。其实,高血压与糖尿病与子宫内膜癌并无直接关系。肥胖、高血压和糖尿病可能都是因为下丘脑-垂体-肾上腺功能失调或代谢异常所造成的后果。同时,垂体促性腺功能也可能不正常,造成无排卵,无孕激素分泌,使子宫内膜长期受到雌激素的持续刺激。有人认为,绝经前的肥胖,尤其从年轻时就肥胖者也是内膜癌的高危因素,因为肥胖者常伴有相对的黄体期孕激素分泌不足,或同时伴有月经不调甚至闭经。
4.晚绝经 据有关报道,绝经年龄>52岁者子宫内膜癌的危险性是45岁以前绝经者的1.5~2.5倍。晚绝经者后几年并无排卵,只是延长了雌激素作用时间。
初潮晚(初潮延迟)对子宫内膜癌是个保护作用,尤其对绝经前的妇女。初潮晚可使内膜癌的危险性减少50%。初潮延迟可以减少雌激素对子宫内膜持续性的刺激作用。
5.多囊卵巢综合征(polycystic ovary syndrome) 在40岁以下的内膜癌的患者中,大约19%~25%患有多囊卵巢综合征。多囊卵巢综合征的患者卵巢滤泡持续时间长,但不能成熟而达到排卵,使子宫内膜处于持续的雌激素刺激之下,缺乏孕酮的调节和周期性内膜脱落,导致内膜发生增生改变。多囊卵巢综合征的患者体内雄激素水平也增高,比一般人约增高3~4倍,而雄激素可转化为雌酮,导致内膜增生或增殖症,进而可发生不典型增生甚至子宫内膜癌。患多囊卵巢综合征的女孩,以后发生内膜癌的可能性是正常月经同龄女孩的4倍。
6.卵巢肿瘤 产生雌激素的卵巢肿瘤,如颗粒细胞瘤和卵泡膜细胞瘤。约25%的纯泡膜细胞瘤并发子宫内膜癌。
7.外源性雌激素 许多研究指出了应用雌激素替代治疗和子宫内膜癌的关系。应用雌激素替代治疗者患内膜癌的机会是不用替代治疗的3~4倍,危险性大小与雌激素剂量,特别是用药时间有关。用较高剂量雌激素大于10年者,患内膜癌的机会较不用者提高了10倍。在无孕酮拮抗或孕酮量不足时,雌激素长期替代治疗会导致内膜增生,甚至癌变。在长期应用雌激素替代治疗的性腺功能不全或Turner综合征的年轻患者就有内膜癌的报道。近年来,在应用雌激素替代治疗时,每个周期均加用至少10天孕激素,则又中和了雌激素长期应用的致癌作用,使其安全性明显增加。因此,雌激素加孕激素的(结合雌激素)的替代治疗,如果孕激素的保护作用足够的话,即使长期应用也是安全的。但也有人持反对意见,认为即使是结合雌激素,如长期应用,对子宫内膜仍有不良影响。并建议对长期应用替代治疗者,应密切追踪子宫内膜的情况,必要时行内膜活检。
近年来,作为乳腺癌的辅助治疗他莫昔芬的应用已日渐增多。在Fornander等的一篇报道里,对1800名患乳腺癌的瑞典妇女进行了调查,用他莫昔芬长达2年以上者,与无辅助治疗或只用化疗者相比,子宫内膜癌的发生率前者是后者的2倍。而应用他莫昔芬长达5年者,内膜癌的发生率是不用者的5倍。
由于他莫昔芬的微弱雌激素样作用,在动物实验中也观察到了对小鼠刺激子宫内膜增生的作用。
8.子宫内膜不典型增生 Kurman等回顾性分析了170例子宫内膜增生患者的刮宫标本,平均随访13.4年,其结果是:1%单纯增生发展为癌,3%复合增生发展为癌,8%非典型单纯增生发展为癌,29%非典型复合增生发展为癌,有非典型增生者,如手术切下子宫,有25%同时伴有分化较好的内膜癌。因此,不典型增生具有癌变倾向,属于癌前病变。
9.其他因素 家族史,有卵巢癌、肠癌或乳腺癌家族史者,患内膜癌的可能性较无家族史者高。经济条件较好,尤其高脂肪饮食者,也是子宫内膜癌的高危人群。在美国有人作过对照研究发现,子宫内膜癌在文化水平高,经济收入高的妇女中的发病率比文化水平低,经济收入少者明显的升高。但也有人认为,可能是前者应用雌激素替代疗法较普通,时间也长且肥胖之故。一般说来,子宫内膜癌在经济发达国家发病率高于不发达国家,在城市的发病率高于农村。
发病因素是否与种族不同有关尚无定论。Matthews等在1997年的一篇回顾性分析中指出,子宫内膜癌在白人妇女中发病率较黑人妇女高。但黑人妇女患内膜癌者,其存活率低,病死率高。子宫内膜的浆液性乳头状癌及透明细胞癌在黑人妇女较白人妇女多见,而子宫内膜癌的这两个亚型常表现为低分化及临床晚期,因此预后差。其原因尚不明确,已知突变的p53基因的过度表达在黑人妇女明显高于白人妇女。
饮食习惯,脂肪、碳水化合物及蛋白质摄入过多均可引起肥胖,而增加体育锻炼,绿色蔬菜和水果有明显的保护作用。
(二)发病机制
子宫内膜癌由米勒管上皮发生而来。肿瘤组织多数形成类似子宫内膜腺上皮的腺癌结构,但亦可形成米勒管上皮多向分化的其他组织类型的结构。病理组织学上表现出女性生殖道各种不同部位的组织类型的形态特征,并依此而分型命名。
1.肉眼表现 子宫内膜癌的组织学类型虽然很多,但各种不同组织类型的癌大体表现没有明显差别。癌组织在子宫内膜呈局限性生长或弥漫侵犯子宫内膜大部或全部。局限型病变多位于子宫底部和宫角附近,后壁较前壁多见。早期局部内膜表面粗糙,无肿块形成,此时检查子宫标本时要特别注意宫角,因病变不明显,诊刮时不易刮到此处。当肿瘤向宫腔内生长时,形成息肉状或菜花状肿块(图1)。肿瘤向肌层生长浸润时,形成坚实的肿块,浸润深浅不一(图2,3),肿瘤与肌层间界限清楚。子宫体积增大或不增大。癌组织灰白色,粗糙质脆或鱼肉状,可伴有灶状出血,分化好的癌肉眼不见坏死,但分化差的癌较常见坏死。有的肿瘤表面形成坚实平面,有时伴有溃疡形成。少数病例癌可沿黏膜表面浸入宫颈管,甚至深达宫颈间质层,也可侵入输卵管。
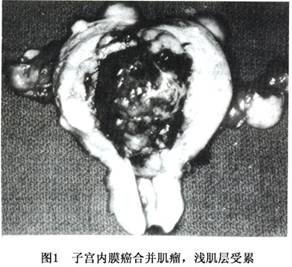
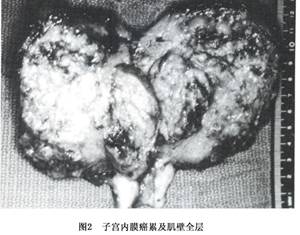
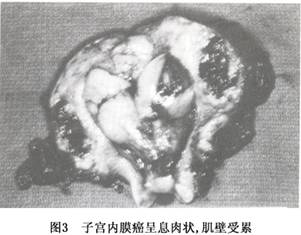
2.组织发生学和组织学类型
(1)组织发生学:女性生殖道器官和组织是由胚胎时期的米勒管发育、演变、分化而来,米勒管乃由体腔上皮内陷而形成。因此,米勒管上皮具有分化形成输卵管、子宫、宫颈及阴道穹隆上皮的多向分化能力。出生后,这些胚胎时期的未分化细胞仍保留在成熟机体的生发层组织内,具有增生及多向分化潜能。正常生理情况下,生发层细胞只显现单向分化,维持该组织细胞的新生与衰亡的替代。病理条件下,如向肿瘤分化时,生发层未分化细胞可显示增生、分化不良和多向分化潜能,形成与原该处组织不同类型的米勒管上皮分化的组织。因此在女性生殖道器官或组织发生癌时,不但可形成与原组织相同类型的癌组织,即子宫内膜样腺癌,而且可以出现米勒管上皮分化为其他部位组织类型的癌,如浆液性腺癌、透明细胞腺癌、黏液性腺癌、鳞状细胞癌、混合性癌及未分化癌等。
(2)组织学类型:由于子宫内膜癌保留有米勒管多向分化潜能,因此癌的发生常出现多种分化的组织成分。各种成分出现几率很不一致,大多数癌组织只有一种与子宫内膜腺体相似的腺癌成分,称子宫内膜样腺癌,或完全由米勒管向子宫内膜以外的女性生殖道其他部位分化的另一种组织类型的癌细胞构成,以致出现与子宫内膜腺体不同组织类型的癌,如浆液性腺癌、透明细胞腺癌、黏液性腺癌、鳞状细胞癌等。有时在子宫内膜样腺癌中可以出现不同比例类型的癌成分。当第二种类型癌的成分超过10%时,则称为子宫内膜混合性癌。当癌细胞处于完全未分化阶段,没有向任何组织类型分化的癌时称为未分化癌。现列出WHO国际肿瘤组织学分类(第二版,1994)提出的子宫内膜癌的分类如下(scully等,1994)表1。

现分述如下:
①子宫内膜样腺癌(endometrioid carcinoma):
A.子宫内膜样腺癌(endometrioid adenocarcinoma):是最常见的一型,占子宫内膜癌的3/4,子宫内膜腺癌的80%~97%。癌组织分化好时,其组织结构与增生期的宫内膜腺体相似,但细胞及腺体结构均有一定的非典型性。细胞呈柱状或矮柱状,核长圆形,染色质较粗较深染,胞浆少,核仁明显,排列紧密,呈假复层;腺体大小不等,形态不规则,或背靠背,或腺腔共壁,或呈筛状腺腔结构,向间质浸润。癌组织分化差时,细胞异型性较大,呈实性条索状或弥散片状排列,构成非鳞状的实性区(图4)。
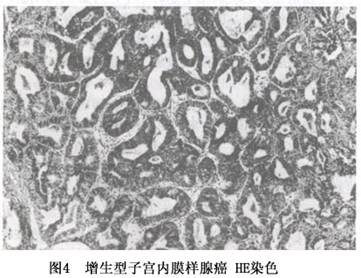
子宫内膜样腺癌的组织学分级:依上述癌的分化程度分为3级,在各级子宫内膜样腺癌中,以高分化型最常见,Ⅰ、Ⅱ、Ⅲ级癌的发生率分别为50%、35%和15%。
约1/4癌内可见细长或短的乳头状或绒毛腺状结构,则应根据癌细胞的形态特征,与下述浆液性乳头状腺癌和透明细胞乳头状腺癌鉴别。后两种癌更具侵袭性,预后更差。
子宫内膜样腺癌有两个变异型:
a.分泌型(secretory type):少见,占宫内膜样腺癌的1%~2%。此型子宫内膜样腺癌的组织结构和形态与分泌早期的宫内膜腺体相似(图5),其发生可能为孕激素刺激的结果。
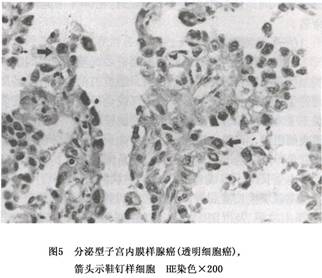
b.纤毛细胞型(ciliated cell type):此型子宫内膜样腺癌的癌细胞大多数都有纤毛。
B.子宫内膜样腺癌伴鳞状分化(endometrioid adeno-carcinoma with squamous differentiation):依子宫内膜样腺癌中鳞状成分的分化程度不同分为:
a.子宫内膜样腺癌伴鳞状化生:指癌内的扁平上皮成分是良性者,过去称子宫内膜腺棘皮癌,但WHO肿瘤国际组织学分类第二版建议不再用此名称。
b.子宫内膜样腺癌伴鳞状分化:指癌内的扁平上皮成分是恶性者,过去称子宫内膜腺鳞癌(图6),WHO第二版分类中也建议不用;若用子宫内膜样腺癌伴鳞癌分化,也是很明确的。
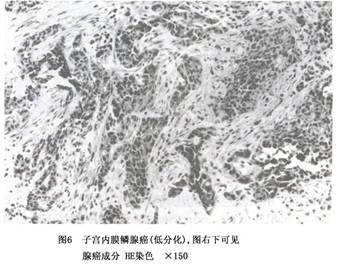
“透明细胞癌”归属于子宫内膜腺癌伴鳞状分化的亚型(WHO,1994,第二版)。
此型子宫内膜样腺癌伴鳞状分化的癌的分级,是根据腺癌成分的分级标准来确定的,并依此判断其预后。过去曾有报道,子宫内膜样腺癌伴鳞状化生者,预后较单一的宫内膜样腺癌好。但据Pekin(2001)报道,子宫内膜样腺癌240例无论伴鳞状化生或鳞癌分化,对预后无影响。
②浆液性腺癌(serous adenocarcinoma):子宫内膜的浆液性腺癌,很少见,不到子宫内膜腺癌的10%。其形态特征与输卵管腺癌和卵巢浆液性腺癌十分相似,癌组织常呈复杂的乳头状分支,故常称浆液性乳头状腺癌。其乳头结构突向大小囊腔,乳头中心为纤维组织和血管组成的轴心,轴心宽窄不一,常有水肿或玻璃样变;表面被覆细胞层次不等,分化较差的为立方状或矮柱状细胞,细胞核常呈高度非典型性,约半数病例有多核、巨核或畸形核,核分裂多,常见灶性坏死,约1/3的病例有沙粒体形成(图7)。分化好的癌乳头分支明显,可见次级分支或细胞性芽或簇;分化差的癌乳头融合,或排列成实性片状。此癌侵袭性强,常浸润肌层及其中的淋巴管或血管,易转移到脊柱内,确诊时常已广泛播散。此型癌即使细胞分化好,其侵袭力也强,约有一半病例,在临床Ⅰ期,手术时已有盆腹腔的播散。
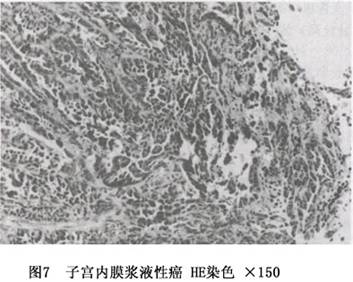
③透明细胞腺癌(clear cell adenocarcinoma):少见,约占子宫内膜癌的1.5%~5%。此腺癌的形态特征是由胞浆透明、富含糖原的透明细胞和鞋钉样细胞构成;透明细胞经组织化学PAS-酶消化后仍阳性,电镜观察细胞质内有大量糖原聚积(图8),证明癌细胞之所以透明,系因含大量糖原所致;鞋钉细胞的特征是细胞基底部细长,顶端膨大,内含1~2个大而深染的核,突起于上皮层表面,或突向腺腔(图9)。癌细胞的排列结构,可呈实性片状、管囊状、乳头状,或这些结构的混合。
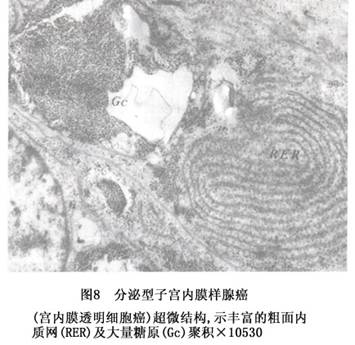
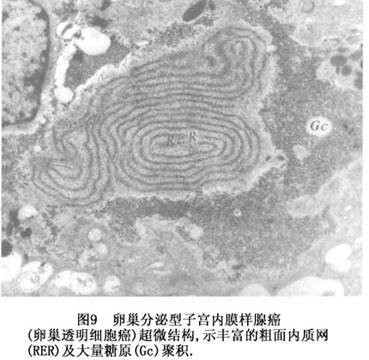
透明细胞腺癌也常有早期播散的倾向。
当透明细胞腺癌呈乳头状结构时,应注意与浆液性乳头状腺癌区别,其要点在于上面所述癌细胞的形态特征。
透明细胞腺癌也可发生在阴道、宫颈和卵巢。发生在阴道或宫颈者,常与其母使用己烯雌酚(diethylstilbestrol)有关,但发生在子宫者未见其有相关性。
若宫颈和宫体同时均有透明细胞腺癌,很难判断何处为原发癌。
④黏液性腺癌(mucinous adenocarcinoma):此腺癌细胞为高柱状或杯状,胞浆富含黏液,核位于基底部;细胞单层或复层构成大小、形状不一的弯曲腺体,有的癌细胞向腔内生长,形成折叠突起的乳头样结构,有的腺腔扩张呈囊状,癌细胞向间质浸润。组织化学用阿尔辛兰、黏液卡红及PAS-酶消化,可见癌细胞胞浆和腺腔内黏液物质均呈阳性反应。
此型腺癌的形态特征与宫颈黏液腺癌和卵巢黏液腺癌十分相似,故在诊断子宫内膜原发的黏液性腺癌之前,必须排除由宫颈管黏膜或卵巢的黏液性腺癌扩散到子宫内膜的可能性。要排除宫颈是否为原发部位,主要靠分段刮宫诊断。也要与子宫内膜腺体的黏液化生相区别,化生是良性病变,而黏液性腺癌的细胞有非典型性,细胞复层化,并向间质浸润。
“黏液表皮样癌”属子宫内膜黏液性腺癌的变异型(WHO,1994,第二版)。黏液性腺癌常属高分化癌,其预后较浆液性腺癌和透明细胞腺癌好。
⑤鳞状细胞癌(squamous cell carcinoma):此癌由不同分化程度的鳞状细胞组成。原发于子宫内膜的鳞状细胞癌罕见。肿瘤多发生在子宫内膜的柱状上皮发生扁平上皮化生的基础上。多见于老年妇女,因绝经后萎缩的子宫内膜常发生老年性子宫内膜炎,或因老年妇女宫颈阻塞,子宫腔积脓及慢性发炎伴扁平上皮化生。少数严重的病例整个子宫内膜被扁平上皮替代,即所谓的子宫鱼鳞癣。
在诊断子宫内膜鳞状细胞癌时,必须具备以下两点:
A.癌内没有腺癌成分,否则为子宫内膜腺癌伴鳞癌分化。
B.子宫内膜鳞状细胞癌不是转移性癌;即宫颈内没有鳞状细胞癌存在,或即使宫颈有鳞状细胞癌,也必须与子宫内膜的鳞状细胞癌没有任何相连关系,与宫颈扁平上皮也无关连。
鳞状细胞癌的亚型中有“疣状癌”(WHO,1994,第二版)。
⑥混合性癌(mixed carcinoma):子宫内膜癌中有两种或更多上述组织类型的癌同时存在,并且其中一种癌至少要占全肿瘤的10%时,称为子宫内膜混合性癌。分类和分级则根据占优势的成分而定,次要成分的类型、分级及所占比例均应在病理诊断中注明。
前面所列的子宫内膜腺样癌伴鳞状分化的癌,曾称为腺鳞癌(或鳞腺癌),不属混合性癌(WHO,1994,第二版)。
混合性癌的确诊应根据子宫切除标本的检查作出,但若是活检小标本,只要出现第二种类型的癌,无论数量的多寡也足够做出混合性癌的诊断(WHO,1994,第二版)。
⑦未分化癌(undifferentiated carcinoma):此癌十分少见。其特点是不具备或只有轻度分化成上述的任何一种细胞类型或结构的癌。此癌几乎全由实性结构组成,癌细胞的非典型性显著,核分裂数多,恶性程度高。未分化癌包括小细胞、大细胞、巨细胞及梭形细胞型,它们也可以不同比例混合存在。
小细胞型未分化癌:含有嗜银细胞。电镜下见癌细胞呈腺上皮分化。诊断小细胞未分化癌应除外:A.神经内分泌癌:其组织化学染色黏液阴性;免疫组化轴突素(Syn)、嗜铬颗粒蛋白(CgA)及神经特异性烯醇化酶(NSE)均呈阳性;电镜下细胞内有神经内分泌颗粒。B.上述的各型子宫内膜腺癌内可有数量不等的嗜银细胞,仍应诊断为原来类型的子宫内膜癌,但应将其中所含嗜银细胞的数量加以说明,而不能用“嗜银细胞癌”一词(WHO,1994,第二版)。小细胞未分化癌侵袭性强。
大细胞、巨细胞及梭形细胞型的未分化癌:黏液染色阳性;电镜下见癌细胞呈腺上皮分化。应除外以下肿瘤:A.子宫绒毛膜上皮癌,免疫组化绒毛膜促性腺激素(HCG)阳性。B.鳞状细胞癌的低分化型或变异型,也可出现类似的大细胞或梭形细胞,但电镜下可见张力原纤维或桥粒。C.低分化肉瘤:免疫组化波形蛋白(Vim)阳性;若怀疑平滑肌肉瘤,免疫组化,结蛋白(Des)、肌动蛋白(Actin)等阳性。
此外,根据观察,不少学者提出或赞成依据各类型癌的病因、病理和临床生物学行为不同,而将子宫内膜癌分为两型,即Ⅰ型和Ⅱ型(sivridis等,2001),现列表2比较如下。
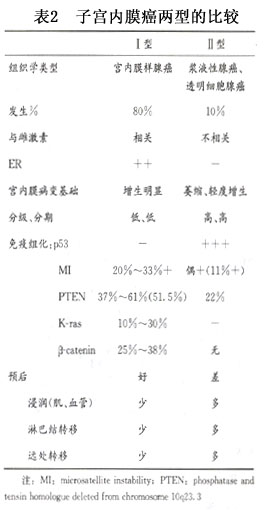
除上述WHO(1994)提出的子宫内膜癌的7种类型外,近年在一些医学文献上报道一些极为罕见的子宫内膜肿瘤类型,如:A.肝样腺癌:以往文献报道2例,治疗无效,2001年又报道1例,甲胎蛋白(AFP)阳性,经手术加化疗(cytoxan、adriamycin及cisplatium方案)有效,8年无复发(Adams等,2001);B.子宫内膜的卵黄囊瘤:报道1例,治疗后有复发(Talerman,2002);C.子宫内膜癌伴滋养叶细胞分化,HCG阳性;D.嗜酸性细胞癌(oxyphilic cell carcinoma),癌细胞大而嗜酸性,为构成癌的主要或惟一成分;E.性索样分化的癌(sertoliform differentiation);F.移行细胞癌等。
4.子宫内膜癌的癌前病变和原位癌 子宫内膜的非典型增生是癌前病变,已被广泛接受。据文献报道,不同类型的子宫内膜增生其癌变率差异较大,单纯性增生的癌变率为1%~10%、复杂性增生为3%~22%、非典型增生为29%~57%。所报道的癌变间隔时间差异较大(1~26年不等),但总的倾向是单纯性子宫内膜增生的癌变间隔时间较非典型增生的长,前者约长于6年,后者约短于5年。
子宫内膜原位癌:对原位癌的确切定义,尚无统一的认识。但原位癌的腺上皮细胞具有明显的异型性,而无浸润,这两点的认识是统一的。对无浸润的部位有两种理解:一是未浸润到子宫内膜的间质,即癌变的腺上皮细胞未突破基底膜。这种情况与重度非典型增生极难区别,就像宫颈的CINⅢ一样,将重度(Ⅲ级)非典型增生和原位癌放在一起称EINⅢ(intra-endometrial neoplasiaⅢ)。另一种理解是已癌变的腺上皮细胞已侵入子宫内膜的间质,但未侵入肌层。这种情况,可能称之为子宫黏膜内癌,更切合实际,表明癌变的腺上皮细胞已侵出基底膜到子宫内膜间质内,而未侵到肌层。一般都认为早期的子宫内膜间质的浸润不易识别,以下病变有所帮助:①浸润到间质内的癌细胞引起间质纤维细胞增生反应,进而胶原化(desomplasia);②浸润处常有炎细胞或泡沫细胞反应。免疫组化的应用也有帮助:①纤维连结蛋白(fibronectin)、Ⅳ型胶原和组织化学网织纤维等染色可见腺体基底膜缺失,表明有浸润发生。②细胞间连接(MRPl/CD9)和细胞与基底膜间连接(integrin)的表达,在癌内低于非典型增生。③细胞外基质糖蛋白(tenasin)和胞质与胞膜骨架连接酶(egrin)的表达,在癌内高于非典型增生。
4.子宫内膜癌的转移 多数子宫内膜癌生长缓慢,局限于内膜或宫腔内时间较长,部分特殊病理类型(浆液性乳头状腺癌,鳞腺癌)和低分化癌可发展很快,短期内出现转移,主要转移途径为直接蔓延、淋巴转移,晚期可有血行转移。
(1)直接蔓延:癌灶初期沿子宫内膜蔓延生长,向上可沿子宫角延至输卵管,向下可累及宫颈管及阴道。若癌瘤向肌壁浸润,可穿透子宫肌壁,累及子宫浆肌层,广泛种植于盆腹膜,直肠子宫陷凹及大网膜。
(2)淋巴转移:为子宫内膜癌主要转移途径。当癌肿累及宫颈、深肌层或分化不良时易早期发生淋巴转移。转移途径与癌肿生长部位有关,宫底部癌灶常沿阔韧带上部淋巴管网,经骨盆漏斗韧带转移至卵巢,向上至腹主动脉旁淋巴结。子宫角或前壁上部病灶沿圆韧带淋巴管转移至腹股沟淋巴结。子宫下段或已累及子宫颈癌灶,其淋巴转移途径与宫颈癌相同,可累及宫旁、闭孔、髂内外及髂总淋巴结。子宫后壁癌灶可沿宫骶韧带转移至直肠淋巴结。约10%内膜癌经淋巴管逆行引流累及阴道前壁(图10)。
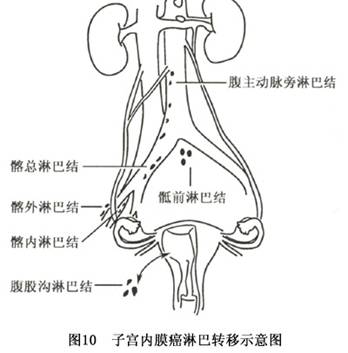
(3)血行转移:晚期患者经血行转移至全身各器官,常见部位为肺、肝、骨等。


